אינסייטק קיבלה אישורי FDA ו-CE למערכת החדשה
5 דצמבר, 2024
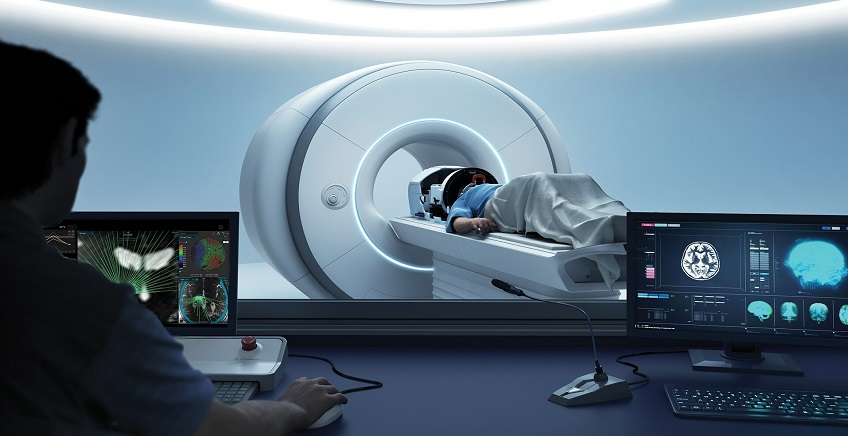
המערכת, המשמשת לטיפול ברעד ראשוני ובתסמינים של פרקינסון, עושה שימוש בקרינת אולטרה-סאונד ממוקדת. המערכת מותאמת לעבוד בממשק למערכות MRI של פיליפס
חברת אינסייטק (Insightec) מחיפה הודיעה כי קיבלה אישור שיווק מה-FDA בארצות הברית ואישור שיווק באירופה (CE Mark) למערכת החדשה שהחברה השיקה בתחילת השנה, Exablate Prime, המשמשת לטיפול תסמונת רעד ראשוני ובתסמינים של פרקינסון, ואשר פועלת בשילוב עם מערכות MRI נבחרות של חברת פיליפס.
לדברי החברה, המערכת החדשה מתבססת על עשור של מחקר ופיתוח והיא מספקת מספר שיפורים משמעותיים בהשוואה למערכת הקיימת, Exablate Neuro, אשר תורמים לדיוק וליעילות של הפרוצדורה. המערכת החדשה נוסתה בבית חולים רמב"ם בישראל ובאוניברסיטה לבריאות ומדע של אורגון, ארצות הברית.
הרעיון מבוסס על העובדה שקרינת אולטרה-סאונד בריכוז נמוך יכולה לעבור דרך רקמות הגוף בלא לפגוע בהן, אולם כאשר היא ממוקדת בנקודה מסויימת, היא גורמת לחימום התאים ולהריסתם, בדומה למיקוד קרני השמש באמצעות עדשה. המערכת משמידה את הרקמות במוח הגורמות להפרעת התנועה ולהפחית את מידת הרעד ולשפר את היכולת המוטורית של המטופל.
השיפורים של הגרסה החדשה מתמקדים גם ברמת החומרה וגם ברמת התוכנה, והם כוללים ממשק משתמש ידידותי יותר, אלגוריתמיקה שנועדה לסייע לרופא לבצע את הפרוצדורה בצורה מדויקת יותר, שילוב של בקר טמפרטורה המתבסס על אלגוריתמים חיזויים כדי לשפר את יעילות מתן הטיפול, וכן שיפורים בתחומי אבטחת המידע, התכנון המקדים, פתרון בעיות ויזואליזציה וניהול הסריקות.
פורסם בקטגוריות: חדשות , מכשור רפואי
פורסם בתגיות: CR , FDA , אינסייטק , פרקינסון , רעד ראשוני
